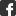Münchener Forscher klären Krankheitsmechanismus auf
Frühe Schäden bei Multipler Sklerose sind umkehrbar

Bei Multipler Sklerose attackieren Immunzellen (grün) die Nervenfasern oder Axone (blau). Die Aufnahme stammt aus dem Rückenmark einer Maus.
27.03.2011, Aktuelle Meldungen
Auf welche Weise Nervenfortsätze bei Multipler Sklerose geschädigt werden, haben jetzt Wissenschaftler der Technischen Universität München und der Ludwig-Maximilians-Universität München herausgefunden. Die bislang unbekannte Form der Nervenschädigung, die „Fokale Axon-Degeneration“, ist in ihrem Frühstadium umkehrbar. Daher hoffen die Münchener Forscher, dass dort zukünftige Therapien greifen könnten. Sie berichten über ihre Untersuchungen in der Online-Version der Zeitschrift Nature Medicine am 27.03.2011.
Das Immunsystem soll Krankheitserreger und Giftstoffe im Körper beseitigen. Zu Autoimmunerkrankungen kommt es, wenn stattdessen körpereigenes Material angegriffen wird. Eines der häufigsten autoimmun bedingten Leiden ist die Multiple Sklerose, kurz MS. Die Symptome sind vielfältig: Manche Patienten drohen zu erblinden, viele können sich nicht mehr richtig bewegen, Arme oder Beine fühlen sich taub an oder kribbeln, bei anderen funktioniert die Blase nicht mehr richtig.
Wie stark diese und andere Symptome zu bleibenden Einschränkungen der Patienten führen, hängt davon ab, wieviele Nervenzellfortsätze oder Axone im Krankheitsverlauf geschädigt werden. Bisher gingen Wissenschaftler davon aus, dass zunächst die Isolierung der Nervenfortsätze, die Myelinscheide, zerstört wird, bevor die Nervenzellfortsätze selbst angegriffen werden.
Chemische Radikale attackieren Zellen
Das Münchener Forscherteam um Prof. Thomas Misgeld von der TU München und Prof. Martin Kerschensteiner vom Klinikum der Ludwig-Maximilians-Universität München fand jedoch heraus, dass bei an MS erkrankten Mäusen auch geschädigte Axone häufig noch von einer intakten Myelinscheide umhüllt sind. Für die Schädigung der Axone ist, so die Erkenntnis der Forscher, ein bislang unbekannter Mechanismus verantwortlich: Die „focal axonal degeneration“, kurz FAD.
Derzeit unterscuhen die Forscher, wie genau die FAD abläuft. Sauerstoff- und Stickstoffradikale spielen wohl eine entscheidende Rolle als Auslöser des Axonzerstörung: Die Radikale werden von Immunzellen produziert und attackieren die „Kraftwerke“ der Zellen in den Nervenzellfortsätzen, die Mitochondrien. Die Folge: Die Nervenzellfortsätzen sterben ab.
In einem frühen Stadium allerdings ist das Absterben der Nervenzellfortsätze umkehrbar. Möglicherweise, so vermuten die Wissenschaftler, könnte dies zur vorübergehenden spontanen Besserung der Beschwerden beitragen, die für MS charakteristisch ist.
Ansatzpunkt für zukünftige Therapien
Dies gibt auch Hoffnung für neue Therapien: Zumindest im Tiermodell konnten die Münchener Mediziner diese Radikale durch Medikamente neutralisieren und so die Erholung vorgeschädigter Axone verbessern. Weiterführende Untersuchungen an menschlichem Gewebe, die in Zusammenarbeit mit Spezialisten der Universitäten Göttingen und Genf erfolgten, lieferten vielversprechende Ergebnisse: Die charakteristischen Stadien des neu gefundenen Degenerationsprozesses lassen sich auch im Gehirn von menschlichen Patienten mit Multipler Sklerose nachweisen, so dass die Behandlungsstrategie auch hier eine Wirkung zeigen könnte.
Bis zu einer möglichen Therapie ist es allerdings noch ein weiter Weg, denn die in den Versuchen eingesetzten Wirkstoffe sind für einen klinischen Einsatz nicht spezifisch und vor allem nicht verträglich genug. „Bevor geeignete therapeutische Strategien entwickelt werden können, müssen wir außerdem erst im Detail klären, wie die Schädigung auf molekularer Ebene abläuft“, sagt Kerschensteiner. „Dabei wollen wir auch untersuchen, ob verwandte Mechanismen in den chronischen Stadien der Multiplen Sklerose eine Rolle spielen.“
Förderung:
Die Arbeit wurde entscheidend von der Deutschen Forschungsgemeinschaft (DFG), unter anderem im Rahmen des SFB 571 (Autoimmunerkrankungen: Von den Manifestationen über die Mechanismen zur Therapie) und des Emmy-Noether Programms gefördert. Auch die Gemeinnützige Hertie-Stiftung, der größte private Förderer der Hirnforschung in Deutschland, und die Alexander-von-Humboldt-Stiftung haben maßgeblich zur Finanzierung des Projekts beigetragen. Weiterhin entstand die Untersuchung im Rahmen des Exzellenzclusters "Center for Integrated Protein Science Munich" (CIPSM) und des BMBF-Kompetenznetzwerks "Multiple Sklerose". Prof. Thomas Misgeld ist „Fellow“ des Institute for Advanced Study der Technischen Universität München (TUM), einer Ideenschmiede der TUM, die mit Mitteln der Exzellenzinitiative gegründet wurde.
Publikation:
http://www.nature.com/nm/journal/vaop/ncurrent/index.html
Ansprechpartner:
Prof. Thomas Misgeld
Lehrstuhl für Biomolekulare Sensoren
Institut für Neurowissenschaften
der Technischen Universität München
Tel.: 089 / 4140 3512
E-mail: thomas.misgeld@lrz.tum.de
Prof. Martin Kerschensteiner
Instititut für Klinische Neuroimmunologie
Klinikum der Universität München
Tel.: 089 / 2180 78282
E-mail: Martin.Kerschensteiner@med.uni-muenchen.de
Kontakt: presse@tum.de