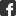Echtzeitmessung von einzelnen Molekülen in einem biologischen Schlüsselprozess
Biophysiker enthüllen Proteinfaltungsdynamik
19.01.2010, Pressemitteilungen
Damit Eiweiße in unserem Körper ihren Dienst tun können, müssen sie sich zu einer genau definierten, dreidimensionalen Struktur zusammenfalten. Funktioniert diese Faltung nicht, kann dies schwere Erkrankungen zur Folge haben. Wie die Proteine in ihre dreidimensionale Form gelangen ist eine der wichtigsten Fragen der Biowissenschaften und der Medizin. Viele Details dieses Prozesses sind jedoch noch ungeklärt. Biophysiker der Technischen Universität München (TUM) haben nun eine Methode entwickelt, mit der sie die Proteinfaltung am Beispiel eines Reißverschluss-ähnlichen Eiweißes in bisher nie erreichtem Detailgrad beschreiben können. In der aktuellen Ausgabe der Proceedings of the National Academy of Sciences (USA) berichten sie über ihre Ergebnisse.
Fehlfunktionen in der Proteinfaltung spielen eine entscheidende Rolle bei vielen schweren Krankheiten, darunter Diabetes, Krebs, Mukoviszidose, Prionenerkrankungen und Alzheimer. Ein besseres Verständnis des Faltungsprozesses ist wichtig, um die Kette der Ereignisse von der DNA-Kodierung bis zur biologischen Funktion zu verstehen. Darauf aufbauend könnten dann gezielt wirksame Medikamente entwickelt werden. Viele vorangegangene Studien – einschließlich Experimenten der selben Arbeitsgruppe mit Rasterkraftmikroskopie – haben versucht, die Energieschwellen zu charakterisieren, die zwischen dem ungefaltetem und gefaltetem Zustand eines Proteins bestehen. Detaillierte Beobachtungen des sehr schnellen Übergangs von einem Zustand in den anderen waren aber bisher kaum möglich. Die aktuellen Ergebnisse öffnen nun die Tür zu höher auflösenden, direkten Messungen.
Das publizierte Experiment ist das neueste in einer langen Serie von biophysikalischen Experimenten mit einzelnen Molekülen die von Professor Matthias Rief und seinen Kollegen im Physik-Department der TUM durchgeführt wurden. Die Ko-Autoren Christof Gebhardt und Thomas Bornschlögl sind Mitarbeiter in Riefs Labor; Gebhardt ist außerdem Mitarbeiter im Exzellenzcluster Munich Center for Integrated Protein Science.
Als Modell für die Echtzeitstudie der Proteinfaltung wählten die TUM Wissenschaftler einen aus Hefe isolierten so genannten Leucin-Zipper. Er hat eine – für ein Protein – relativ einfache Struktur und einen Faltungsvorgang ähnlich dem eines Reißverschlusses. „Man stelle sich zwei parallele Ketten von Aminosäuren vor, unten zusammengeschlossen, oben offen,“ erläutert Matthias Rief. „Wie bei einem Reißverschluss lagern sich dann die beiden offenen Enden zusammen.“
Die Forscher erweiterten diese Struktur so dass sie unabhängige Messungen am oberen, unteren und mittleren Teil des Reißverschlusses machen konnten. Die freien Enden am oberen Teil hielten sie mit Griffen aus doppelsträngiger DNA fest. Die DNA-Griffe wiederum waren an kleine Perlen gebunden, die die Forscher direkt mit einer “optischen Pinzette” manipulieren konnten. Dieses Werkzeug basiert auf der Fähigkeit eines Laserstrahls mit einem speziellen Profil, Objekte im Nanobereich festhalten zu können. Ein Ende des Proteinmoleküls wurde so fixiert. Das andere stand zwar unter Spannung, hatte aber so viel Bewegungsfreiheit, dass die Faltungsdynamik direkt und in Echtzeit gemessen werden konnte. Dieser Aufbau ermöglichte Messungen mit hoher Auflösung, in der Distanz sowie in der Zeit. “Wir können tausende von Zwischenstufen vermessen und erstmals nicht nur Anfangs- und Endzustand anschauen sondern auch die Berge dazwischen,” fasst Rief die Ergebnisse zusammen.
Original-Publikation:
Full distance resolved folding energy landscape of one single protein molecule,
J. Christof M. Gebhart, Thomas Bornschlögl, and Matthias Rief,
PNAS Early Edition for the week of Jan. 18, 2010.
Kontakt:
Prof. Matthias Rief
Technische Universität München
Lehrstuhl für Experimentalphysik (E 22)
James-Franck-Str. 1, D 85748 Garching
Tel: +49 89 289 12471
Fax: +49 89 289 12523
E-Mail - Internet
Kontakt: presse@tum.de
Mehr Information
| 100119_zipper_pw_de.pdf |
Druckansicht der Presseinformation (DE),
(Type: application/pdf,
Größe: 130.2 kB)
Datei speichern
|
|
| 100119_zipper_en.pdf |
Printable version of the press release (EN),
(Type: application/pdf,
Größe: 126.9 kB)
Datei speichern
|