Neue Erkenntnisse zur Bewegung molekularer Motoren:
Mini-Transporter auf Abwegen
26.04.2012, Pressemitteilungen
Kinesine übernehmen in unseren Zellen eine lebenswichtige Funktion: Die kleinen Laufmaschinen transportieren entlang langer Proteinfasern wichtige Substanzen und sorgen für eine effektive Infrastruktur. Biophysiker der Technischen Universität München (TUM) und der Ludwig Maximilians Universität München (LMU) haben nun herausgefunden, dass manche Transporter beim Laufen ähnlich wie Autos auf einer mehrspurigen Autobahn auch die Spur wechseln können. Über den molekularen Mechanismus dieses bislang nicht bekannten Phänomens berichten die Forscher in der aktuellen Ausgabe des Fachmagazins „Molecular Cell“.
Molekulare Motoren sind der Schlüssel zur Entwicklung höherer Lebewesen. Entlang langer Proteinfasern transportieren sie Proteine, Signalmoleküle, Organellen oder sogar ganze Chromosomen gezielt von einem Ort der Zelle zum anderen. Ähnlich wie Lastwagen auf Autobahnen sind ständig Tausende der kleinen Motorproteine gleichzeitig unterwegs – ein hochkoordinierter und äusserst schneller Transport. Nur mit dieser höchst effektiven Infrastruktur konnten sich größere, komplexere Zellen und vielzellige Organismen bilden – eine Fähigkeit die beispielsweise Bakterien fehlt, da diese weder molekulare Motoren noch ein Cytoskelett besitzen.
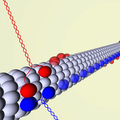
Eine besondere Klasse molekularer Motoren sind die Kinesine. Sie bestehen aus zwei miteinander verdrillten Eiweißketten. Jede Kette besitzt einen Kopf, der an der Oberfläche des Mikrotubulus andocken kann, eine Halsdomäne sowie eine Stiel- und eine Schwanzdomäne, an deren Ende die Fracht angehängt wird. Das Kinesin bewegt sich, indem es abwechselnd einen Kopf vor den anderen setzt. Das erste umfassend erforschte Kinesin ist das Kinesin-1, das eine Vielzahl von aufeinanderfolgenden Schritten ausführt ohne sich vom Mikrotubulus abzulösen. Dabei bewegt es sich auf seinem langen Weg exakt geradeaus und bleibt dabei stets auf einer einzigen Faser des Mikotubulus, der sich aus 13 röhrenförmig angeordneten Einzelfasern zusammensetzt.
Wissenschaftler um Zeynep Ökten, Arbeitsgruppenleiterin am Lehrstuhl für Biophysik der Technischen Universität München und Melanie Brunnbauer, Doktorandin am Lehrstuhl für Biophysik, haben nun erstmals demonstriert, daß Kinesine während des Transports auch ihre Spur wechseln können. Die Wissenschaftlerinnen haben die Stelle im Kinesin-Protein identifiziert, die bestimmt ob ein Kinesintyp geradeaus läuft oder sich spiralförmig bewegt. Es ist ein Strukturelement der Halsdomäne. „Ist die Halsregion stabil, haben die beiden Köpfe des Kinesins nur eine geringe Reichweite. Das Kinesin kann keine Seitenschritte machen und läuft geradeaus“, sagt Ökten. „Destabilisiert man jedoch die verantwortliche Region, vergrößert sich die Reichweite der Köpfe und das Motorprotein kann die Faser wechseln und sich spiralförmig um den Mikrotubulus herum bewegen.“
Um die neue Erkenntnis zu überprüfen bauten die Wissenschaftlerinnen bestimmte Aminosäurereste in die verantwortliche Region ein, eine Art molekularer Schalter, mit dem sie die Reichweite der beiden Köpfe regulieren können. Das Ergebnis war deutlich: Destabilisierten sie die Halsregion des Kinesin-1 Motors und vergrößerten so die Reichweite der beiden Köpfe, geriet das sonst so vorbildlich geradeaus laufende Kinesin-1 plötzlich von seiner Bahn und lief spiralförmig. Ahmten sie durch eine chemische Querverbindung eine stabile Halsregion nach, konnten sie das Protein wieder dazu bringen geradeaus zu laufen.
Zu den neuen Ergebnissen gelangten Ökten und Brunnbauer durch einen einzigartigen Versuchsaufbau: Sie brachten zwei 3 Mikrometer große Kunststoffperlen in eine Lösung ein und fixierten jede mit einem Laserstrahl, einer sogenannten „optischen Pinzette“. Dann legten sie in Präzisionsarbeit ein Mikrotubulusstück dazwischen. Im letzten Schritt fixierten sie ein mit Motorproteinen eines bestimmten Kinesin-Typs umhülltes weiteres Kügelchen ebenfalls mit einem Laserstrahl und setzten es vorsichtig auf den Mikrotubulus auf.
Sobald sie nun den dritten Laserstrahl deaktivierten lief das Motorprotein los und die Wissenschaftlerinnen konnten den Weg des Moleküls unter dem Mikroskop live mitverfolgen. „Auf diese Weise konnten wir erstmals die Bewegung eines Motortyps direkt beobachten“, erklärt Ökten. „Als wir zum ersten Mal die trudelnde Bewegung eines Kinesin-2 Proteins sahen, lachten wir alle – die Bewegung war so klar und deutlich, man musste einfach nur hinschauen und alle Zweifel waren verflogen.“ Dieser Versuchsaufbau erlaubt den molekularen Motoren sich frei zu bewegen und kommt so den realen Verhältnissen in der Zelle sehr viel näher als frühere Untersuchungsmethoden.
Mit dem neuen Versuchsaufbau untersuchten Ökten und Brunnbauer die Laufbahnen einer ganzen Reihe verschiedener Kinesin-2 Proteine aus unterschiedlichen Organismen – mit überraschendem Ergebnis: Entgegen der bisher in der Wissenschaft vorherrschenden Annahme, dass sich Kinesine typischer Weise geradeaus bewegen, zeigten fast alle Kinesine Spiralbewegungen, in vielfältigen Variationen. „Dies zeigt uns, dass die Spiralbewegung in der Natur keineswegs eine Ausnahme ist, sondern die Regel“, erklärt Ökten. „Man sollte sich vielmehr fragen, warum die Evolution überhaupt eine Geradeausbewegung hervor gebracht hat, wie wir sie beim Kinesin-1 beobachten können. Das ist wirklich außergewöhnlich.“ In weiteren Forschungen möchten die Wissenschaftler um Ökten und Brunnbauer den Sinn der unterschiedlichen Bewegungsarten genauer untersuchen.
Die Forschung wurde gefördert aus Mitteln der Deutschen Forschungsgemeinschaft (DFG, SFB 863). Einen besonderen Dank sprechen die Autoren in der Publikation auch Brunnbauers kleinem Sohn und dessen Babysitterin aus. Im Arbeitskreis der Biophysik an der TU München fand Melanie Brunnbauer die Flexibilität und Unterstützung, um ihre Arbeit auch nach der Geburt ihres Kindes fortzuführen. Ihre erfolgreiche Forschungsarbeit ist ein Beleg dafür, dass Familie und Beruf auch in der molekularbiologischen Forschung gut vereinbar sind – wenn die Voraussetzungen stimmen.
Originalpublikation:
Torque Generation of Kinesin Motors Is Governed by the Stability of the Neck Domain, Melanie Brunnbauer, Renate Dombi, Thi-Hieu Ho, Manfred Schliwa, und Zeynep Ökten, Molecular Cell (2012), doi: 10.1016/j.molcel.2012.04.005
Kontakt:
Dr. Zeynep Ökten
Physik Department E22
Technische Universität München
James-Franck-Str. 1
85748 Garching
Tel.: +49 89 2180 75898
E-Mail
Kontakt: presse@tum.de
Mehr Information
| Kinesine_spiral.avi |
Kinesin 2 (Z. Ökten/M. Brunnbauer / Cell),
(Type: video/x-msvideo,
Größe: 1.8 MB)
Datei speichern
|
|
| KInesine_straight.avi |
Kinesin 1 (Z.Ökten/M. Brunnbauer / Cell),
(Type: video/x-msvideo,
Größe: 966.7 kB)
Datei speichern
|
|
| 120426_Kinesine_PW_DE.pdf |
Druckversion dieser Pressemitteilung (DE),
(Type: application/pdf,
Größe: 101.4 kB)
Datei speichern
|
|
| 120426_Kinesine_PW_EN.pdf |
Printable version of the press release (EN),
(Type: application/pdf,
Größe: 95.6 kB)
Datei speichern
|