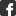Eine molekulare Maschine bei der Arbeit
Schutz vor Stress durch Hsp90
22.02.2009, Pressemitteilungen
Wenn Zellen in Stress geraten, leistet das Eiweiß Hsp90 einen wichtigen Beitrag dazu, dass sie überleben. Die Arbeitsweise dieses Proteins haben nun zwei Gruppen der Technischen Universität München (TUM) aufgeklärt. Die Ergebnisse werden in zwei Artikeln der aktuellen Online-Ausgabe des renommierten Wissenschaftsmagazins Nature Structural and Molecular Biology publiziert.
Proteine sind die Maschinen der Zelle. Sie erfüllen vielfältige Aufgaben, wie zum Beispiel den Transport von Molekülen, die Bewegung von Muskeln, die chemische Umwandlung von Stoffen oder auch die Faltung anderer Proteine. Das so genannte Hitzeschockprotein Hsp90 ist für unsere Zellen von zentraler Bedeutung, da es viele grundlegende Prozesse steuert. Es ist zum Beispiel maßgeblich daran beteiligt, dass einfache Aminosäureketten zu funktionierenden Proteinen mit einer genau definierten räumlichen Struktur gefaltet werden. Vor allem dann, wenn die Zelle durch Hitze, Vergiftungen oder Sauerstoffmangel hohem Stress ausgesetzt ist, wird das Protein vermehrt hergestellt, um die Schäden in Grenzen zu halten.
Die notwendige Energie für seine Funktion gewinnt Hsp90 durch die langsame Spaltung von ATP. Dabei ändert sich die Gestalt des Proteins. Wie bei einer makroskopischen Maschine bewegen sich einzelne Teile gegeneinander, allerdings nur um einige Nanometer. Zwei Arbeitsgruppen der TUM, um Professor Johannes Buchner aus der Chemie und Professor Thorsten Hugel aus der Physik, haben diese scherenartige Bewegung nun zum ersten Mal in Echtzeit verfolgt und die einzelnen Schritte des Reaktionsmechanismus aufgeklärt.
Um diese Veränderungen im Nanometerbereich überhaupt verfolgen zu können, wurden zwei fluoreszierende Farbstoffmoleküle an exakt definierten Stellen im Protein angebracht und als molekulares Lineal benutzt: Beleuchtet man einen Farbstoff, so bringt dieser den zweiten Farbstoff umso heller zum Leuchten, je näher er an diesem ist. Mit Hilfe dieser Technik (FRET) konnte sogar die Bewegung einzelner Hsp90 Moleküle analysiert werden.
Wichtige und unerwartete Ergebnisse sind zum Einen, dass der Prozess in einer Reihe von wohl definierten Teilschritten abläuft und dass nur ein Teil der Energie in mechanische Arbeit, also Bewegung, umgesetzt wird. Interessanterweise beeinflussen Helferproteine die Kopplung zwischen „Kraftstoffverbrauch“ und Bewegung im Protein. Die Bewegung wird dabei beschleunigt oder gebremst.
Diese Ergebnisse sind nicht nur für das grundsätzliche Verständnis von molekularen Maschinen von Bedeutung, sondern auch für die Pharmaforschung, da Hsp90 ein interessantes Zielprotein für die Krebstherapie ist. Wenn es gelänge, die Maschine kontrolliert abzuschalten, dann könnte man die Teilung von Krebszellen stoppen.
„Diese beiden Arbeiten zeigen sehr schön, wie wichtig inzwischen die interdisziplinäre Zusammenarbeit geworden ist und wie gut sie hier auf dem Campus funktioniert,“ sagt Buchner. „Hier haben die beiden TUM Departments Physik und Chemie, die beiden Exzellenzcluster CIPSM und NIM sowie das Zentralinstitut für Medizintechnik (IMETUM) aufs engste zusammengearbeitet. Für eine einzelne Arbeitsgruppe sind solche Ergebnisse nicht zu erzielen.“
Die Arbeiten wurden durch die Deutsche Forschungsgemeinschaft (SFB 594), den Fonds der Chemischen Industrie und die beiden Exzellenzcluster Nanoinitiative München (NIM) und Munich Center for Integrated Protein Science (CIPSM) unterstützt.
Originalpublikationen:
Martin Hessling, Klaus Richter, Johannes BuchnerDissection of the ATP-induced conformational cycle of the molecular chaperone Hsp90
Nature Structural & Molecular Biology, 16, 287 - 293 (2009)
http://dx.doi.org/10.1038/nsmb.1565
Moritz Mickler, Martin Hessling, Christoph Ratzke, Johannes Buchner, Thorsten Hugel
The large conformational changes of Hsp90 are only weakly coupled to ATP hydrolysis
Nature Structural & Molecular Biology, 16, 281 - 286 (2009),
http://dx.doi.org/10.1038/nsmb.1557
Bildmaterial:
http://mediatum2.ub.tum.de/node?id=683843Links:
Film zur Proteinfaltung durch Chaperone wie das Hsp90 (© MPI für Biochemie; Film benötigt Quicktime)Homepage Arbeitskreis Prof. Buchner
Homepage Arbeitskreis Prof. Hugel
Ansprechpartner:
Prof. Dr. Johannes BuchnerTechnische Universität München
Department Chemie
Lichtenbergstr. 4, 85747 Garching
Tel.: 089 289 13341
Fax: 089 289 13345
Prof. Dr. Thorsten Hugel
Technische Universität München
Physik Department
James Franck Str. 1, 85748 Garching
Tel.: 089 289-16781
Kontakt: presse@tum.de
Mehr Information
| 090222_hsp90_pw |
Presseinformation,
(Type: application/pdf,
Größe: 208.1 kB)
Datei speichern
|