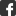Kontrolliertes Recycling in der Zelle:
TUM-Wissenschaftler entdecken Erkennungs-Mechanismus beim Protein-Abbau
22.05.2008, Press releases
Ständig werden in lebenden Zellen Eiweiße auf- und wieder abgebaut. Das zentrale Werkzeug zum Abbau nicht mehr benötigter Proteine ist das so genannte Proteasom. Wissenschaftler der Technischen Universität München (TUM) identifizierten in Zusammenarbeit mit Kollegen aus den Universitäten Minnesota (USA) und Frankfurt sowie der Harvard Medical School (USA) einen lang gesuchten Rezeptor am Proteasom, der zum Abbau vorgesehene Eiweiß-Moleküle erkennt. Erstmals konnte die dreidimensionale Struktur der Bausteine und der Mechanismus der Erkennung aufgeklärt werden. Die Untersuchung der Abbaumechanismen soll Strategien liefern, mit denen Erkrankungen wie Krebs, Alzheimer oder auch Mucoviszidose bekämpft werden können. Die Forschungsarbeit wird heute in der aktuellen Ausgabe von „Nature“ veröffentlicht.
Eiweiße oder Proteine sind die zentralen Bausteine lebender Zellen. Bei Bedarf werden sie aufgebaut und nach getaner Arbeit müssen sie zügig wieder abgebaut werden. Hierfür verfügt die Zelle über ein ausgeklügeltes Recycling-System: Nicht mehr benötigte Eiweiße werden mit einem kleinen Protein namens Ubiquitin markiert. Solche als „Abfall“ markierten Bausteine werden dann im zentralen „Müllschredder“ der Zelle, dem Proteasom, in kurze Stücke zerhackt.
Das Proteasom ist ein aus 28 Untereinheiten aufgebauter, stabiler Zylinder. Eine Art Deckel verhindert, dass Proteine zufällig hinein geraten und zerstört werden. Ein Schleusensystem im Deckel erkennt als Abfall markierte Bausteine. Es spaltet die Ubiquitin-Markierung ab, faltet die verschlungene Eiweißkette auf und befördert sie in den Schredder. Den TUM-Wissenschaftlern ist es nun erstmals gelungen, die dreidimensionale Struktur von Rpn13 zu bestimmen, einer Schlüsselkomponente des Schleusensystems.
Alles deutet darauf hin, dass die Forscher hierbei einen besonderen Kontrollmechanismus entdeckt haben: Fälschlicherweise markierte Proteine tragen meist nur ein oder zwei Ubiquitin-Markierungen. Eiweiße, die definitiv nicht mehr benötigt werden, tragen eine Kette mit mehreren Ubiquitin-Einheiten. Markierte Proteine docken nun mit dem Ubiquitin-Rest an Rpn13 an. Das Besondere an diesem Rezeptor: Auf einer Seitenkette sitzt ein Enzym, das Ubiquitin-Einheiten abschneidet. Trägt das an den Rezeptor andockende Protein nun nur wenige Ubiquitin-Moleküle, so werden diese abgeschnitten und das Protein kommt wieder frei. Besitzt das Protein eine längere Ubiquitinkette, reicht das Abschneiden der Ubiquitin-Einheiten nicht aus. Es bleibt am Rezeptor hängen und wandert in den Schredder.
Als die Wissenschaftler Proteasome von Säugetieren und Hefezellen verglichen stellten sie fest, dass die Hefezellen den beschriebenen Mechanismus nicht besitzen. „Dieser Kontroll-Mechanismus scheint sich im Laufe der Evolution erst bei höheren Lebensformen heraus gebildet zu haben,“ sagt Michael Groll, Professor für Biochemie an der TU München. Überraschender Weise zeigten Hefezellen, denen Rpn13 fehlte, keine nennenswerten Unterschiede zu gesunden Zellen, die über die Rpn13-Einheit verfügt. Die Forscher schließen daraus, dass es neben dem beschriebenen noch weitere Ubiquitin-Erkennungssysteme geben muss, die die Funktion von Rpn13 ausgleichen können. Denn für einen Organismus wäre es fatal, wenn er nur einen Ubiquitin-Rezeptor besäße. Krankheitserreger könnten diesen umgehen, und der Organismus wäre dann hilflos ausgeliefert.
„Trotz weltweitem Interesse ist über die verschiedenen Kontrollmechanismen des Proteasoms bisher nur wenig bekannt. Und dies, obwohl das Protein-Recycling einer der wichtigsten zelluären Prozesse überhaupt ist,“ erläutert Michael Groll. So spielt die unwiederbringliche Zerstörung beim Wachstum benötigter Proteine wahrscheinlich eine zentrale Rolle für die Entwicklung von der embryonalen Stammzelle zur Herzmuskel- oder Nervenzelle. Bei Krankheiten wie Alzheimer oder bei Prionen-Infektionen entstehen Protein-Verklumpungen. Auch hier könnte die gezielte Beeinflussung der Abbaumechanismen völlig neue Strategien gegen die Krankheiten ermöglichen. Ein vom Proteasom gesteuerter Prozess wird bereits bei der Krebstherapie genutzt: Krebszellen sind darauf angewiesen, schneller zu wachsen als die sie umgebenden normalen Zellen. Bremst man die Aktivität des Proteasoms mit einem Medikament, so werden alle Zellprozesse verlangsamt. Bestrahlt man nun die Zellen, so werden die auf schnelles Wachstum angewiesenen Krebszellen stärker geschädigt als die gesunden daneben.
Die in der aktuellen Ausgabe der Zeitschrift „Nature“ veröffentlichte Arbeit wurde durch die Deutsche Forschungsgemeinschaft (SFB 740 und Exzellenzcluster 115 „Macromolecular Complexes“) und die National Institutes of Health (USA) gefördert.
Veröffentlichung:
Ubiquitin docking at the proteasome through a novel pleckstrin-homology domain interaction, Patrick Schreiner, Xiang Chen, Koraljka Husnjak, Naixia Zhang, Suzanne Elsasser, Daniel Finley, Ivan Dikic, Kylie J. Walters and Michael Groll, Nature, Vol. 453, S. 548-552, 22. Mai 2008: http://www.nature.com/nature/journal/v453/n7194/#lt
Links:
Editor’s Summary: http://www.nature.com/nature/journal/v453/n7194/edsumm/e080522-07.html
Nature News and Views: http://www.nature.com/nature/journal/v453/n7194/#nv
Nature Podcast: http://www.nature.com/nature/podcast/index.html
Kontakt:
Prof. Dr. Michael Groll
Lichtenbergstraße 4
D-85748 Garching
Tel.: 089 289 13360
Fax: 089 289 13363
E-Mail: Michael.Groll@ch.tum.de
Kontakt: presse@tum.de
More Information
| rpn13-ubi-pdf |
Kontrolliertes Recycling in der Zelle - Presseinformation,
(Type: application/pdf,
Size: 111.6 kB)
Save attachment
|
|
|
|
rpn13-ubi-bild |
Rpn13-Rezeptor mit angelagertem Ubiquitin - Bild, Im Eingangsbereich des zellulären „Müllschredders“, dem Proteasom, wacht der Rezeptor Rpn13 (rotes Bändermodell) darüber, dass nur Eiweiße geschreddert werden, die tatsächlich nicht mehr gebraucht werden. Er erkennt die Ubiquitin-Einheiten (blaues Oberflächenmodell), mit denen die Zelle zu entsorgende Proteine markiert. Bild: Michael Groll,TU München; 10x10 cm, 300 dpi
(Type: image/jpeg,
Size: 197.1 kB)
Save attachment
|