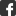Doppelte Salzbrücke entscheidend für Funktion des Proteins p53
Doppelbrücke schützt vor Krebs
09.09.2005, Pressemitteilungen
Molekulare Veränderungen der Zellstruktur, genauer Mutationen an bestimmten Genen, sind häufig die Ursache, weshalb normale gesunde Zellen sich in bösartige Tumorzellen verwandeln können. Das Gen p53 gehört in diese Kategorie, sein Protein p53 fungiert als unser “Genomwächter“.
Wenn DNA-Schäden vorliegen, zum Beispiel durch intensive Sonnenbestrahlung der Haut, stoppt es die Zellteilung und verschafft der Zelle ausreichend Zeit, die Schäden zu reparieren. Sind die Schäden zu groß, sorgt p53 dafür, dass die Zelle „Selbstmord“ begeht und schützt damit andere vor Entartung.
In 50 Prozent aller menschlichen Tumoren ist p53 mutiert und damit nicht funktionstüchtig. Die meisten p53-Mutationen betreffen dessen DNA-Bindungsstelle oder destabilisieren das Protein. Daneben existieren aber auch Mutationen in einem kurzen, helixförmigen Abschnitt, die nur indirekt die DNA-Bindefähigkeit beeinflussen. Prof. Horst Kessler, Ordinarius für Organische Chemie der TU München in Garching und Leiter des Bayerischen NMR-Zentrums wies mit seinem Team aus TUM-Chemikern und der Penzberger Pharmaforschung der Roche Diagnostics GmbH an verschiedenen p53-Mutanten nach, dass eine doppelte Salzbrücke in dieser Region von p53 für die Funktionstüchtigkeit verantwortlich ist.
Das Wissenschaftler-Team erzeugte zielgerichtet verschiedene Mutationen in diesem Abschnitt und untersuchte die Mutanten auf ihre DNA-Bindefähigkeit. Als besonders aufschlussreich erwiesen sich Mutationen der Aminosäure-Positionen 180, die in „gesundem“ p53 durch den negativ geladenen Glutaminsäurerest (Glu) besetzt ist, und 181, in der der positiv geladene Rest Arginin (Arg) sitzt. Sind durch Mutation beide Positionen durch dieselbe Aminosäure, Glutamin oder Arginin, besetzt, bindet p53 nicht mehr an die DNA, obwohl diese beiden Positionen gar nicht direkt an die DNA gebunden sind. Das Geheimnis steckt in den Ladungen. In „gesundem“ p53 ziehen sich zwei p53-Moleküle über diese Reste. Es bildet sich eine so genannte doppelte Salzbrücke, die beide p53 Moleküle zusammenhält und damit die DNA-Bindung stabilisiert. Kehrt man dagegen eine der Ladungen um, so können sich die beiden p53 Moleküle nicht mehr aneinanderheften und damit auch nicht an die DNA binden. Die DNA und Störungen innerhalb derselben werden dann nicht mehr erkannt.
Diese Resultate sind ein weiterer Puzzlestein für die außerordentlich komplexe Wirkungsweise der Kontrolle krebsrelevanter Doppelstrangbrüche, wie sie z.B. durch Einwirkung von Licht hervorgerufen werden.
Kontakt:
Prof. Horst Kessler, Lehrstuhl II für Organische Chemie
Tel: 089/289-13300, Kessler@ch.tum.de
Kontakt: presse@tum.de